Daftar isi :
I. Anfis intestinum minor
II. Konsep dasar
A. Pengertian penyakit
B. Etiologi
C. Pathofisiologi
D. Manifestasi klinis
E. Pemeriksaan diagnostic
F. Penatalaksanan medis
G. Komplikasi
H. Prognosis
I. Epidemiologi
III. Asuhan keperawatan
A. Pengkajian
B. Diagnose
C. Intervensi
IV. Jurnal
V. Satuan Acara Penyuluhan tentang penatalaksanaan penyakit stenosis usus halus
VI. Daftar pustaka
I. Anfis intestinum minor
Usus halus atau usus kecil adalah bagian dari saluran pencernaan yang terletak di antara lambung dan usus besar. Usus halus terdiri dari tiga bagian yaitu usus dua belas jari (duodenum), usus kosong (jejunum), dan usus penyerapan (ileum). Pada usus dua belas jari terdapat dua muara saluran yaitu dari pankreas dan kantung empedu
Di dalam usus dua belas jari, dihasilkan enzim dari dinding usus. Enzim tersebut diperlukan untuk mencerna makanan secarakimiawi:
Enterokinase, untuk mengaktifkan tripsinogen yang dihasilkan pankreas menjadi tripsin;
Erepsin atau dipeptidase, untuk mengubah dipeptida atau pepton menjadi asam amino;
Laktase, mengubah laktosa menjadi glukosa dan galaktosa;
Maltase, berfungsi mengubah maltosa menjadi glukosa;
Disakarase, mengubah disakarida menjadi monosakarida;
Peptidase, mengubah polipeptida menjadi asam amino;
Lipase, mengubah trigliserida menjadi gliserol dan asam lemak;
Sukrase, mengubah sukrosa menjadi fruktosa dan glukosa.
Di dalam usus penyerapan (iluem) terdapat banyak lipatan atau lekukan yang disebut jonjot-jonjot usus (vili). Vili berfungsi memperluas permukaan penerapan, sehingga makanan dapat terserap sempurna
Makanan yang berupa glukosa, asam amino, vitamin, mineral, air akan diserap pembuluh darah kapiler di vili, dan diangkut ke hati ke vena porta. Di dalam hati, beberapa zat akan diubah ke bentuk lain dan beberapa lainnya akan diedarkan ke seluruh tubuh.
Sedangkan asam lemak dan gliserol diangkut melalui pembuluh limfa.
Duodenum
Disebut juga usus dua belas jari, dibagian duodenum terdapat papilla vateri. Dinding duodenum mempunyai lapisan mukosa yang banyak mengandung kelenjar yang disebut kelenjar burner, befungsi untuk memproduksi getah intestinum.
Duodenum adalah bagian pertama dari usus kecil dan menghubungkan perut ke jejunum, yang merupakan bagian kedua dari usus kecil
Jejunum dan ileum
Sambungan antara jejunum dan ileum tidak memiliki batas yang tegas. Ujung bawah ileum berhubungan dengan sekum dengan perantara lubang yang bernama orifisium ileosekalis. Orifisium ini diperkuat oleh sfingter ileosekalis dan pada bagian ini terdapat katup valvulo sekali yang berfungsi untuk mencegah cairan dalam kolon asendens tidak masuk kembali pada ileum.
Mukosa usus halus
Permukaan epitel yang sangat kuat melalui lipatan mukosa dan mikrovili memudahkan pencernaan dan absobsi. Lipatan ini dibentuk oleh mukosa dan submukosa yang dapat memperbesar permukaan usus. Pada penampang melintang, vili dilapisi oleh epitel dan kripta yang menghasilkan bermacam-macam hormone jaringan dan enzim yang memegang peran aktif dalam pencernaan.
Fungsi usus halus
1. Menerima zat-zat makanan yang sudah dicerna untuk diserap melalui kapiler-kapiler darah dan saluran-saluran limfe.
2. Menyerap protein dalam bentuk asam amino
3. Karbohidrat diserap dalam monosakarida.
II. Konsep Dasar
Pengertian
Stenosis adalah suatu obstruksi lengkap dengan lubang kecil sekunder diafragma atau web, sedangkan atresia adalah sebuah obstruksi lengkap.
Stenosis duodenum adalah penyempitan atau striktura lumen duodenum yang abnormal menyebabkan obstruksi yang tidak lengkap. Bedakan dengan atresia yang menyebabkan obstruksi lengkap Stenosis dan atresia duodenum umumnya terdapat pada bagian pertama dan kedua duodenum, kebanyakan pada daerah sekitar papilla Vater. Saluran empedu utama dapat berhubungan dengan mukosa intraluminal web.
Stenosis jejunum dan ileum adalah penyempitan atau striktura lumen jejunum dan ileum yang abnormal menyebabkan obstruksi yang tidak lengkap.
Stenosis intestinum minor adalah sebuah penyempitan pada bagian-bagian usus halus yaitu duodenum, ileum dan jejunum yang merupakan penyakit kelainan bawaan yang menyebabkan obstruksi tidak lengkap.
Etiologi/penyebab
– kompresi dari permukaan duodenum oleh band-band Ladd sekunder untuk rotasi lengkap dari usus
– Annular membungkus pancreas
– keturunan resesif autosomal
– Adanya Polyhidramnion ( saat kehamilan )
–
Factor resiko
1. Kelainan Kromosom
Kelainan genetik pada suami atau istri dapat menimbulkan kelainan kongenitalpada anaknya. Dengan kemajuan teknik dalam menyelidiki secara langsung bentuk dan jumlahkromosomdalam sel – sel manusia, maka dapat ditemukan hubungan antara kelainan dalam jumlah serta bentukkromosomdan kelainan kongenitaltertentu, misalnya kelainan padakromosomautosome
2. Faktor Mekanik
Tekanan mekanik pada janin dalam uterus dapat menyebabkan kelainan bentuk. Bentuk kelainan tergantung daerah organ yang mengalami tekanan yang terus menerus,
3. Faktor Infeksi
Infeksi yang dapat menimbulkan kelainan kongenitalialah terutama infeksi oleh virus. Pada masaorganogenesis, yakni dalam triwulan pertama kehamilan, karena infeksi ini menimbulkan gangguan dalam pembentukan alat – alat atau organ dalam tubuh janin.
4. Faktor umur ibu
Kehamilan di usia tua atau mendekati menopouse beresiko lebih tinggi melahirkan anak dengan kelainan kongenitalcacat. Ini diduga karena menurunnya fungsi organ yang mendukung proses kehamilan terutama hormon.
5. Radiasi
Radiasi yang terus menerus pada kehamilan dapat menimbulkan mutasigene, yang dapat menyebabkan kelainan kongenitalpada yang dilahirkan
6. Faktor gizi
Pada ibu hamil yang kekurangan gizi beresiko melahirkan bayi cacat dari pada ibu yang hamil kecukupan gizi. Diduga vitamin A, riboflamin, asam folik, thiamin gizi pendukung pada stadiumorganogenesisdi triwulan pertama.
7. Faktor lain
Banyak kelainan kongenitalyang tidak diketahui penyebabnya, diduga faktor – faktor hipoxia, hipo – hiperthermia dan juga masalah – masalah sosial dapat menyebabkan kelainan kongenital.
Faktor predisposisi
a. Sosial Ekonomi Rendah
Sosial ekonomi rendah ini berhubungan dengan status gizi keluarga. Status gizi keluarga yang kurang akan menyebabkan gangguan pertumbuhan janin, terutama pada masa kehamilan dimana masa ini sangat dibutuhkan asupan gizi yang cukup. Gizi yang cukup sangat diperlukan untuk perkembangan janin.
b. Lingkungan
Lingkungan juga sangat penting untuk mendukung pertukaran dan perkembangan radikal bebas yang sering disebabkan polusi terutama polusi udara. Didaerah – daerah industri dan keadaan lingkungan hidup yang buruk, ini sangat mempengaruhi kesehatan apalagi pada masa – masa awal dari kehidupan.
c. Grande Para ( Usia ibu waktu hamil lebih dari 30 tahun )
Kehamilan diusia tua beresiko lebih tinggi melahirkan anak cacat. Diduga karena menurunnya fungsi organ yang mendukung proses kehamilan, terutama hormon kehamilan.
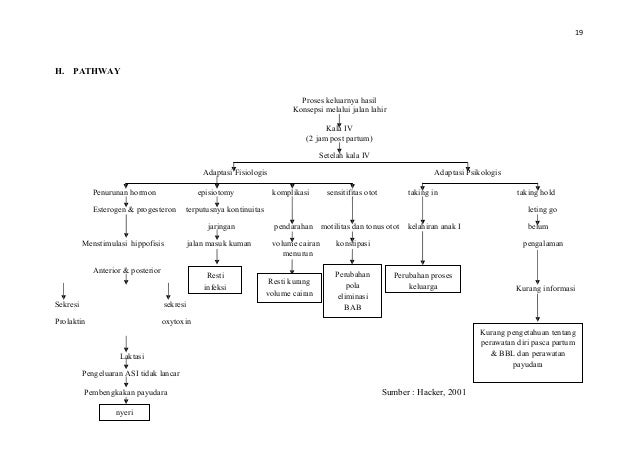
Patofisiologi
Stenosis duodenum adalah penyebab umum dari obstruksi usus pada bayi baru lahir. Hal ini lebih sering terjadi pada dewasa sebagai akibat dari penyakit ulkus peptikum
Stenosis duodenum dapat disebabkan oleh kompresi dari permukaan duodenum oleh band-band Ladd sekunder untuk rotasi lengkap dari usus
Annular membungkus pankreas duodenum dapat menyebabkan stenosis atau obstruksi duodenum
Etiologi dan factor resiko
Perases kehamilan trimester 3 30-60 hari
Masa pembentukan organ tubuh janin
Kegagalan proses vacuolisasi selama periode embryo Biasa bersamaan dengan annular pancreas (1/3 tengah) (duodenum )
- Asuhan kebidanan pada bayi baru lahir dengan bblr pdf uncurbable and preservative. Askep anak dengan diare ppt • Askep bayi prematur dengan bblr.
- Asuhan keperawatan pada bayi s. P dengan prematur/bblr/ se-dang masa kehamilan di ruang neonatologi rsud dr. Soetomo surabaya.
Alat pencernaan bayi prematur masih belum sempurna, lambung kecil. Nur Asnah Sitohang: Asuhan Keperawatan Pada Bayi Berat Badan Lahir Rendah, 2004.
pembuluh darah yang menimbulkan aseptic necrosis intra uterin yang berakhir pada atresia (ileum dan jejunum)
Terjadi stenosis karena adanya etiologi
Antara masa gestasional 8-10 minggu, lumen di duodenum dilengkapi oleh berkumpulnya vakuola-vakuola, dan juga terjadi rekanalisasi. Gangguan selama periode penting dalam perkembangan duodenum dipercaya menyebabkan terjadinya kegagalan rekanalisasi dan menyebabkan terjadinya atresia, stenosis, dan web.
Manifistasi klinis
– saat berumur beberapa bulan/tahun Gejala : Muntah , bilious dan non bilious Bisa timbul saat dewasa : refluks gastroesofageal, ulserasi peptic, atau obstruksi duodenum proksimal dari stenosis oleh bezoar.
– Gejala sering tidak berkembang pada masa neonatus
– Biasanya anak mengalami mual intermiten dengan muntah. Muntahan berisi empedu
– Anak gagal untuk berkembang
– Dapat ditemukan di perut bagian atas kembung.
– Diwarnai empedu muntah pada neonatus berusia 24 jam
– radiografi polos yang menunjukkan penampilan ganda-gelembung gas tanpa distal.
– Gas usus distal mengindikasikan stenosis, membran tidak lengkap, atau anomali duktus hepatopancreatic.
– stenosis duodenum signifikan tidak diobati, kondisi cepat menjadi fatal sebagai akibat dari hilangnya elektrolit dan ketidakseimbangan cairan
Pemeriksaan diagnostic
– Pada riwayat kelahiran, terlambatnya evaluasimekoniumlebih dari 24 jam atau anak tidak bisa defekasi sedangkan anus ada. Pada orang dewasa ada riwayatkonstipasikronik
– Radiodiagnostik (Pemeriksaan fotopolosabdomen, terlihat tanda – tandaobstruksiusus lebih rendah. Umumnya gambarankolonsulit dibedakan dengan gambaran usus halus.)
PEMERIKSAAN FISIK :
PEMERIKSAAN FISIK Inspeksi : tampak contour/ peristalsis lambung atau usus di daerah epigastrium. Palpasi : tampak distended pada daerah epigastrium disebabkan oleh duodenum dan gaster yang berdilatasi
Pada Inspeksi (Distensiabdomen, perut buncit, muntah – muntah warna kehijauan)
Palpasi atau Perabaan (Perabaan padaabdomenterasa bagian – bagian darikolonyang melebar dan bisa dirasakan perut keras atau defansabdomen.)
PEMERIKSAAN PENUNJANG :
PEMERIKSAAN PENUNJANG Pemeriksaan Laboratorium Elektrolit Hematokrit Gula darah Goldah dan crossmatch Pencitraan Foto polos abdomen Barum meal Barium enema Rectal Biopsy
DIFERENSIAL DIAGNOSIS :
DIFERENSIAL DIAGNOSIS Malrotasi yang disertai volvulus Membran atau pita yang melintang dan menekan duodenum
– Plain x-ray dapat menunjukkan perut membesar dengan isi perut dipertahankan, bagian fisrt duodenum dapat melebar
– X-ray setelah menelan barium berisi suatu fluida menunjukkan menunjukkan obstruksi duodenum
– Atas Gastrointestinal Endoscopy (pemeriksaan lingkup fleksibel serat optik) akan menunjukkan obstruksi duodenum (Lihat Panendoscopy)
Penatalaksanaan medis
– Indikasi untuk Bedah
Indikasi ditentukan oleh derajat obstruksi usus Sebuah obstruksi bermutu tinggi biasanya dilakukan pada kebijaksanaan dokter bedah (intervensi bedah elektif)
Tingkat rendah penghalang parsial mungkin pergi bertahun-tahun tanpa membutuhkan pembedahan
Sebagian besar operasi berlangsung di tahun-tahun dewasa dengan operasi sesekali di masa kecil
– Operasi
Pembedahan dilakukan di bawah anestesi umum Sayatan dibuat di perut bagian atas
Stenosis ini biasanya dilewati tanpa menghapus apapun pankreas atau jaringan duodenum. Prosedur memotong berbagai:
– Duodenoduodenostomy – lubang dibuat di sisi duodenum atas dan di bawah stenosis diikuti dengan penjahitan dinding duodenum di lubang bersama untuk membentuk bypass (sisi untuk memotong sisi)
– Duodenojejunostomy – akhir untuk memotong sisi duodenum untuk jejunum
– Gastrojejunostomy – sisi perut bagian bawah ke sisi bypass jejunum
– Gastroduodenostomy – sisi perut bagian bawah ke sisi dari bypass duodenum
– Resusitasi cairan
– Dekompresi dengan NGT
– Antibiotika
Komplikasi
– Intestinal obstruksi e.c
– adhesive Duodenal dismotility
– Megaduodenum dengan sindrom blind loop Refluks duodenogastrik
– gastritis Ulkus Peptic Cholelithiasis
– Komplikasi yang terkait dengan operasi besar mungkin terjadi
o Perdarahan
o Infeksi
o Gangguan pernapasan (kesulitan bernafas)
o Hipotermia (suhu tubuh rendah)
o Rendah urin
o Obstruksi usus
o Fistula – kebocoran pada garis jahitan Pos Operasi dan Perawatan Setelah
Prognosis
Angka bertahan hidup bayi ,bila ditangani dengan baik, adalah 90-95 %. Peningkatan angka bertahan hidup dapat dihubungkan dengan perawatan respirasi, hiperelementasi, anestesi pediatrik yang meningkat hasilnya, peningkatan kewaspadaan dan terapi anomali lain yang mengikuti.
stenosis duodenum signifikan tidak ditangani, kondisinya akan segera menjadi fatal sebagai akibat gangguan cairan dan elektrolit. Sekitar setengah dari neonatus yang menderita stenosis duodenum lahir prematur. Hidramnion terjadi pada sekitar 40% kasus obstruksi duodenum. stenosis duodenum paling sering dikaitkan dengan trisomi 21. Sekitar 22-30% pasien obstruksi duodenum menderita trisomi 21,jantung, ginjal, CNS, dan musculoskeletal.
Epidemiologi
Kasus stenosis duodenal atau duodenal web dengan perforasi jarang tidak terdiagnosis hingga masa kanak-kanak atau remaja.Penggunaan USG telah memungkinkan banyak bayi dengan obstruksi duodenum teridentifikasi sebelum kelahiran. Pada penelitian cohort besar untuk 18 macam malformasi kongenital di 11 negara Eropa, 52% bayi dengan obstruksi duodenum diidentifikasi sejak in utero. Obstruksi duodenum ditandai khas oleh gambaran double-bubble (gelembung ganda) pada USG prenatal. Gelembung pertama mengacu pada lambung, dan gelembung kedua mengacu pada loop duodenal postpilorik dan prestenotik yang terdilatasi. Diagnosis prenatal memungkinkan ibu mendapat konseling prenatal dan mempertimbangkan untuk melahirkan di sarana kesehaan yang memiliki fasilitas yang mampu merawat bayi dengan anomali saluran cerna. Stenosis duodenum 1/5000-10.000 kasus. Rasio atresia dan stenosis adalah 3:2 atau 2:2
1 : 5000–10000, 25–30 % bersamaan dengan Down‘sSyndrome ( Mongolism) )
III. Asuhan keperawatan stenosis intestinum minor
a. Pengkajian
1. Pola nutrisi ( menurut ganer)
a) Pola nutrisi dan metabolik
Penurunan nafsu makan, mual, muntah karena adanya obstruksi gas dan akan meningkatkan tekanan intraabdomen. Pembatasan makanan dari Rumah Sakit diet rendah sisa, bubur.
b) Pola eliminasi BAB
1) Konstipasi ; karena kelemahan peristaltik usus
2) Feces ; konsistensi;skibala
3) Diare ; biasanya terjadi ada penyulit enterokolitis
c) Pola aktifitas dan latihan
1) Aktifitas kebiasaan klien setiap hari
2) Kebutuhan hidup ( ADL) sehari – hari
3) Pekerjaan klien
d) Pola reproduksi dan sexual
1) Tanda – tanda kelamin sekunder, waktu pertama kali menstruasi
2) Tanda – tanda kelamin primer
3) Status klien, bujang, menikah, tidak menikah
e) Pola istirahat dan tidur
Istirahat tidur berkurang, merasakan keadaan sakitnya, setuasi tak adaptif lingkungan rumah sakit
f) Pola persepsi sensori
1) Nyeri : kadang distensiabdomen
2) Sensasi nyeri baik
g) Pola kognitif
1) Daya ingat baik
2) Kesadaran, tergantung sakitnya
h) Pola peran hubungan keluarga
Hubungan keluarga, orang tua, anak, kakak, adik
i) Pola persepsi dan konsep diri
1) Harga diri rendah : adanya citra tubuh yang terganggu
j) Pola koping dan toleransi stress
1) Hobi; untuk mengalihkan perasaan
2) Teman dekat; untuk mencurahkan perasaannya
3) Intro/ exofet; menghadapi masalah
k) Pola nilai kepercayaan
1) kepatuhan beribadah, agama klien
2) hubungan kedekatan dan beribadah menurut klien
2. Pemeriksaan fisik
Abdomen:
I. : Distensiabdomen, perut membuncit
A.: Peningkatan bising usus, karena terjadi sunbatan, pasase usus terganggu
P : Defansabdomen, teraba masaskibala, nyeri
P : Timpani, pekak
B. Diagnose dan Intervensi
1. Gangguan keseimbangan cairan dan elektrolit berhubungan dengan muntah
Tujuan :
– keseimbangan cairan dan elektrolit tidak terganggu
kriteria hasil
– Intake dan output seimbang
– Tidak ada tanda – tanda dehidrasi
Intervensi
– Tanda – tanda vital normal intervensi
– Awasi masukan dan keluaran cairan
– Kaji tanda – tanda dehidrasi
– Kaji tanda – tanda vital
– Catat intake dan output
– Kolaburasi untuk pemberian cairan parenteral
2. Resiko tinggi infeksi berhubungan dengan luka, tindakan infasif ( Carpenito, 1999)
Tujuan :
– Agar tidak terjadi infeksi
Kriteria hasil :
– Luka bersih
– Tidak ada tanda – tanda infeksi
Intervensi :
– Rawat luka secara aseptik dan antiseptik
– Kaji tanda – tanda infeksi
– Kolaburasi gizi untuk pemberian antibiotika
3. Resiko tinggi nutrisi kurang dari kebutuhan berhubungan dengan mual, muntah
Tujuan :
– Agar kebutuhan nutrisi terpenuhi
Kriteria hasil :
– Berat badan seimbang
– Hb dan albumin dalam keadaan normal
Intervensi :
– Kaji penyebab mual, muntah
– Monitor intake makanan
– Berikan situasi makan yang menyenangkan
– Anjurkan untuk makan porsi kecil tetapi sering
– Kolaburasi pemeriksaan Hb dan albumin per minggu
– Monitor berat badan
– Kaji keadaan kulit klien
Privacy and security. Designed with Your Needs in Mind! CDS is built to ensure that our clients' information is secured and kept private. Copernic web search.
SATUAN ACARA PENYULUHAN
(SAP)
Tema : Penyakit stenosis usus halus
Sub Tema : Penatalaksanan Penyakit stenosis usus halus
Sasaran : Keluarga Tn. B
Tempat : Di rumah sakit
Hari/Tanggal : Minggu, 13 November 2011
Waktu : 30 Menit
A. Tujuan Instruksional Umum
Setelah mengikuti penyuluhan selama 30 menit, diharapkan Keluarga Tn. B dapat mengetahui Penatalaksanaan Penyakit stenosis usus halus.
B. Tujuan Instruksional Khusus
Setelah mengikuti penyuluhan selama 30 menit, diharapkan Keluarga Klien Dapat:
• Menjelaskan Latar Belakang Penyakit stenosis usus halus dengan benar
• Menyebutkan penyebab yang dapat menimbulkan Penatalaksanan Penyakit stenosis usus halus
• Menyebutkan tanda/gejala dari Penyakit stenosis usus halus
• Mengerti Patofisiologi Penyakit stenosis usus halus
• Mengerti cara penatalaksanaan Penyakit stenosis usus halus
C. Materi
1. Latar belakang penyakit Penyakit stenosis usus halus
2. Faktor penyebab dari Penyakit stenosis usus halus
3. Tanda/gejala Penyakit stenosis usus halus
4. Patofisiologi Penyakit stenosis usus halus
5. Cara penatalaksanaan Penyakit stenosis usus halus
D. Metode
1. Ceramah
2. Tanya jawab
E. Kegiatan Penyuluhan
No Kegiatan Penyuluh Peserta Waktu
1. Pembukaan • Salam pembuka
• Menyampaikan tujuan penyuluhan
• Menjawab salam
• Menyimak,
Mendengarkan, menjawab pertanyaan 5 Menit
2. Kerja/ isi • Penjelasan pengertian, penyebab, gejala, patofisiologi & Penatalaksanan Penyakit stenosis usus halus
• Memberi kesempatan peserta untuk bertanya
• Menjawab pertanyaan
• Evaluasi • Mendengarkan dengan penuh perhatian
• Menanyakan hal-hal yang belum jelas
• Memperhatikan jawaban dari penceramah
• Menjawab pertanyaan 20 menit
3. Penutup • Menyimpulkan
• Salam penutup • Mendengarkan
• Menjawab salam 5 Menit
F. Media
Leaflet : Tentang penyakit Penyakit stenosis usus halus
G. Sumber/Referens
a. Smeltzer Suzanne C.Buku Ajar Keperawatan Medikal Bedah Brunner & Suddarth. Alih bahasa Agung Waluyo, dkk. Editor Monica Ester, dkk. Ed. 8. Jakarta : EGC; 2001.
b. Doenges M.E. (1989)Nursing Care Plan, Guidlines for Planning Patient Care (2 nd ed ). Philadelpia, F.A. Davis Company.
c. Long; BC and Phipps WJ (1985)Essential of Medical Surgical Nursing : A Nursing Process ApproachSt. Louis. Cv. Mosby Company.
d. http://www.yoursurgery.com/ProcedureDetails.cfm?BR=1&Proc=80
H. Evaluasi
Formatif : Klien dapat menjelaskan latar belakang Penyakit stenosis usus halus
Klien mampu menjelaskan faktor penyebab Penyakit stenosis usus halus
Klien dapat menjelaskan tanda/gejala Penyakit stenosis usus halus
Klien mampu menjelaskan patofisiologi Penyakit stenosis usus halus
Klien mampu mengerti cara Penatalaksanan Penyakit stenosis usus halus
Sumatif : Klien dapat mengetahui Penatalaksanan Penyakit stenosis usus halus
Yogyakarta, Sabtu 12 November 2011
Penyuluh
(Riski Wulandari)
IV. Daftar pustaka
Smeltzer Suzanne C.Buku Ajar Keperawatan Medikal Bedah Brunner & Suddarth. Alih bahasa Agung Waluyo, dkk. Editor Monica Ester, dkk. Ed. 8. Jakarta : EGC; 2001.
Doenges M.E. (1989)Nursing Care Plan, Guidlines for Planning Patient Care (2 nd ed ). Philadelpia, F.A. Davis Company.
Long; BC and Phipps WJ (1985)Essential of Medical Surgical Nursing : A Nursing Process ApproachSt. Louis. Cv. Mosby Company.
http://www.yoursurgery.com/ProcedureDetails.cfm?BR=1&Proc=80
V. Jurnal
BIRTH DEFECT RISK FACTOR SERIES: Atresia-Stenosis of the Small Intestine
DESCRIPTION
Defects of the small intestine include both atresia and stenosis. Atresia involves closure or disconnection of a portion or multiple portions of the small intestine while stenosis is a narrowing, webbing, or incomplete closure of a portion of the small intestine (Garza 2005). Small intestinal atresia/stenosis most frequently affects the duodenum (~50%), followed by the jejunum (~35%); the ileum (~15%) is least likely to be affected (Forrester 2004, Cragan 1993). This defect is usually diagnosed prenatally via ultrasound or shortly after delivery, as the intestinal blockage will cause abdominal distention, difficulty in feeding, and the bowel movements (Garza 2005).
Most cases of small intestinal atresia/stenosis do not occur with other birth defects; the exception to this is duodenal atresia/stenosis (Forrester 2004, Garne 2002, Haeusler 2002, Harris 1995, Cragan 1993, Camilla 1990). Approximately 50% of infants with duodenal atresia/stenosis have another anomaly, including cardiac, genitourinary, or anorectal defects, and annular pancreas (Garza 2005, Bianchi 2000). Duodenal atresia is also associated closely with trisomy 21; however, chromosomal abnormalities are not associated with the jejunum or ileum atresia/stenosis (Haeusler 2002, Torfs 1998, Kallen 1996, Harris 1995, Cragan 1993). A severe form of duodenal atresia/stenosis is described at “apple-peel” deformity. This name is derived from the appearance of the intestine as it spirals around the blood supply and resembles an apple peel (Yamanaka 2000).
EMBRYOLOGY
At approximately week 3 of gestation, the hepatobiliary system and pancreas are developing (Garza 2005). As these organs are forming, the duodenum is a solid structure. Between the 8 th to 10th weeks of gestation, a vacuolation process occurs whereby the duodenum becomes a hollow structure. Failure of the vacuolation process may result in duodenal atresia and stenosis (Sencan 2002). It has also been suggested that small intestinal atresia/stenosis may be due to vascular disruption during development (Werler 2003).
GENETIC FACTORS
Small intestinal atresia/stenosis has been reported to run in families (Gahukamble 2003, Gahukamble 2002). This defect has also been connected with deletions of chromosome 22q11 (most often associated with DiGeorge syndrome) and chromosome 12q24.3 (Doray 2002, Yamanaka 2000). Both of these chromosomes have been tentatively linked to digestive system development. Additionally, an as-yet unidentified portion of chromosome 2p23-p24 has also been suggested as a causal factor for this defect when it is associated with Feingold syndrome (van Bokhoven 2005). Further examination of the chromosome indicated that a microdeletion of the gene MYCN might also contribute to developmental disruption of the digestive system. MYCN is activated by Sonic Hedgehog (Shh) signaling; if a portion of the gene is missing, then Shh signaling is disrupted. This disruption has been shown to cause a variety of defects, including tracheo-esophogeal fistula and esophogeal atresia (van Bokhoven 2005).
Other studies indicate that fibroblastic growth factors (fgf) (signaling molecules that are involved in organogenesis) may contribute to small intestinal atresia/stenosis when they malfunction (Fairbanks 2004, Fairbanks 2003). An absence of specific fibroblastic growth factors or their receptors disrupts the signaling pathways; this disruption may cause several different defects. The authors suggest an autosomal recessive inheritance of this defect (Fairbanks 2004, Fairbanks 2003).
OUTCOME
Small intestinal atresia/stenosis has a variable outcome depending on the location and severity of the defect; the presence of additional defects and/or chromosomal abnormalities also contributes to the probability of survival (Garza 2005). Minor defects can be repaired surgically, and generally the prognosis is good (Garza 2005). However, repair of major defects including multiple intestinal atresias have not been as successful (Bilodeau 2004).
DEMOGRAPHIC AND REPRODUCTIVE FACTORS
With respect to race/ethnicity, several studies have reported small intestinal atresia/stenosis to be more common in African-Americans than in whites (Harris 1995, Cragan 1993). One investigation observed no significant difference in risk of small intestinal atresia/stenosis in infants born to Vietnamese women compared to infants born to non-Hispanic white women in California (Shaw 2002). Another study found that rates for small intestinal atresia/stenosis were higher for Far East Asians than for Caucasians (Forrester 2004). Higher occurrence rates for this defect are not associated with mixed-race ancestry (Yang 2004).
One study failed to identify any secular trends in small intestinal atresia/stenosis over time (Forrester 2004, Cragan 1993). Another found no seasonal variation in intestinal atresia rates (Bound 1989).
Review of the literature failed to identify any studies that examined the relationship between small intestinal atresia/stenosis and geographic location. One investigation failed to identify any association between duodenal atresia or jejunoileal atresia and altitude (Castilla 1999).
The influence of maternal age on small intestinal atresia/stenosis risk has been variously reported to be U-shaped (Forrester 2004, Harris 1995) or higher for women who are less than 20 years of age (Francannet 1996), although one study failed to identify any association between maternal age and these defects (Cragan 1993).
No statistically significant relationship between these conditions and infant sex has been reported (Forrester 2004, Rittler 2004, Haeusler 2002, Harris 1995, Cragan 1993).
Asuhan Keperawatan Stroke
Risk for small intestinal atresia/stenosis increases with lower birth weight and lower gestational age (Rasmussen 2001, Martinez-Frias 2000, Cragan 1993, Mili 1991); however there does not appear to be an increased risk for this defect with large for gestational age infants (Lapunzina 2002). Small intestinal atresia has been associated with intrauterine growth retardation (Khoury 1988). One investigation reported no effect of parity on risk for these defects (Harris 1995). Small intestinal atresia/stenosis is more common among multiple gestation pregnancies (Martinez-Frias 2000, Mastroiacovo 1999, Francannet 1996, Harris 1995, Cragan 1994, Cragan 1993, Ramos-Arroyo 1991), although one study reported no association between plurality and small gut atresia (Kallen 1986).
One study identified higher risk of duodenal atresia with consanguinity (Martinez-Frias 2000), while another found no association between parental consanguinity and intestinal atresia (Rittler 2001). However, two more recent studies have indicated that inherited factors contribute to the etiology of this defect (Gahukamble 2003, Gahukamble 2002). Higher rates of small intestinal atresia/stenosis have been reported in a consanguineous Arab population even in the absence of teratogenic or environmental factors (Gahukamble 2002).
FACTORS IN LIFESTYLE OR ENVIRONMENT
Maternal education does not appear to affect risk for small intestinal atresia/stenosis (Martinez-Frias 2000). One investigation reported no association between parental farming occupation and pesticide exposure and risk of intestinal atresia (Kristensen 1997). Another investigation failed to identify any significant association between either duodenal atresia or jejunoileal atresia and proximity to various types of industry (Castilla 2000). An article that reviewed recent studies of paternal occupation and birth defects reported increased risk of small intestinal atresia and paternal occupation of motor vehicle operator (Chia 2002).
Maternal diabetes, hyperthyroidism, hypothyroidism, and other acute and chronic maternal diseases have not been associated with small intestinal atresia or duodenal atresia, although one study noted increased rates of esophageal/intestinal atresia with preexisting diabetes and gestational diabetes (Aberg 2001). Maternal infectious diseases have been suggested to increase risk for ileal atresia (Martinez-Frias 2000, Francannet 1996, Becerra 1990, Khoury 1989). One investigation reported no association between maternal fever, upper respiratory infection, or allergy and small intestinal atresia/stenosis (Werler 2002).
Prenatal use of vasoconstrictive drugs, including cocaine, amphetamines, decongestants, and nicotine has been associated with intestinal atresia (Werler 2003, Hoyme 1990), although other studies have reported no association between fetal cocaine exposure and birth defects (Behnke 2001). One investigation found elevated rates of small intestinal atresia/stenosis/web with maternal use of pseudoephedrine and pseudoephedrine in combination with acetaminophen (Werler 2002). Thalidomide and hydantoin have been linked to increased risk of duodenal atresia (Jones 1988). One study reported a potential association between methylene blue used during amniocentesis and jejunal atresia (van der Pol 1992). Aspirin, phenylpropanolamine, ibuprofen, antihistamines, guaifenesin, dextromethorphan, vitamins, iron, other minerals, andovulation induction have not been reported to increase risk of small intestinal atresia/stenosis (Werler 2002, Martinez-Frias 2000, Francannet 1996). Studies have reported no association between cephalosporin antibiotics, ampicillin, or thebenzodiazepinesnitrazepam, medazepam, tofisopam, alprazolum, and clonazepam and intestinal atresia/stenosis (Eros 2002, Czeizel 2001a, Czeizel 2001b, Holmes 2001). Exposure to calcium channel blockers (Sorenson 2001), corticosteroids (Park-Wyllie 2000), marijuana (Fried 2000), chemotherapy (Cardonic 2004), and fluoxetine (Prozac™) (Chambers 1996) have not been found to be risk factors for small intestinal atresia/stenosis.
No association between maternal folic acid or multivitamin use and intestinal atresia has been reported (Botto 2004, Czeizel 1996). Furthermore, a study that examined co-trimoxazole, a combination of trimethoprim and sulfamethoxazole that is a folic acid antagonist, failed to find any association between the medication and atresia/stenosis of the small intestine (Czeizel 1990).
Living in proximity to a landfill sites and solid waste incinerators has not been found to be a risk factor for small intestinal atresia/stenosis (Cordier 2004, Harrison 2003).
PREVALENCE
The reported prevalence for small intestinal atresia/stenosis has shown variation between studies, ranging between 0.6 and 3.1 per 10,000 births for duodenal atresia/stenosis and 0.4 and 1.4 for other small intestinal atresia/stenosis (Table 1). Differences in prevalence may be due to differences in case inclusion criteria.
Table 1. Prevalence per 10,000 births of small intestinal atresia/stenosis
Reference Location Time period Rate per 10,000 live births Other* rate Total rate
Texas DSHS 2005 Texas 1999-2002 3.1
Haeusler 2002 Europe 1996-1998 1.0 1.0
Martinez-Frias 2000 Spain 1976-1998 0.6 0.4 1.2
Martinez-Frias 2000 Latin America 1967-1996 0.6 0.5 1.2
Torfs 1998 California , USA 1983-1993 2.3 3.9
Stoll 1996 France 1979-1987 3.0
Harris 1995 France 1976-1990 0.7 0.8
Harris 1995 Sweden 1973-1990 1.1 0.5
Harris 1995 California , USA 1983-1990 1.0 0.9
Papp 1995 Hungary 1988-1990 2.0
Cragan 1993 Georgia , USA 1968-1989 1.4 1.4 2.8
Castilla 1990 Central and South America 1982-1986 0.7 0.6
*Other small intestinal atresia/stenosis
REFERENCES
Aberg A, Westbom L, Kallen B. Congenital malformations among infants whose mothers had gestational diabetes or preexisting diabetes. Early Hum Dev 2001;61:85-95.
Becerra JE, Khoury MJ, Cordero JF, Erickson JD. Diabetes mellitus during pregnancy and the risks for specific birth defects: a population-based case-control study. Pediatrics 1990;85:1-9.
Behnke M, Eyler FD, Garvan CW, Wobie K. The search for congenital malformations in newborns with fetal cocaine exposure. Pediatrics 2001;107:e74.
Bianchi DW, Crombleholme TM, D’Alton ME. Duodenal atresia. In: Fetology: Diagnosis and Management of the Fetal Patient. New York: McGraw-Hill, 2000; pp. 523-529.
Bilodeau A, Prasil P, Cloutier R, Laframboise R, Meguerditchian A, Roy G, Leclerc S, Peloquin J. Hereditary multiple intestinal atresia: thirty years later. Journal of Pediatric Surgery, Vol. 39, No. 5, 2004.
Botto LD, Olney RS, Erickson JD. Vitamin supplements and the risk for congenital anomalies other than neural tube defects. American Journal of Medical Genetics Part C (Semin. Med. Genet.), Vol. 125C, 2004.
Bound JP, Harvey PW, Francis BJ. Seasonal prevalence of major congenital malformations in the Fylde of Lancashire 1957-1981. J Epidemiol Community Health 1989;43:330-342.
Cardonic E, Iacobucci A. Use of chemotherapy during human pregnancy. Lancet, Vol. 5, May 2004.
Castilla EE, Campana H, Camelo JS. Economic activity and congenital anomalies: an ecologic study in Argentina. Environ Health Perspect 2000;108:193-197.
Castilla EE, Lopez-Camelo JS, Campana H. Altitude as a risk factor for congenital anomalies. Am J Med Genet 1999;86:9-14.
Castilla EE, Lopez-Camelo JS. The surveillance of birth defects in South America: I. The search for time clusters: epidemics. In: Advances in Mutagenesis Research. Springer-Verlag, New York. 1990 pp. 191-210.
Chambers CD, Johnson KA, Dick LM, Felix RJ, Jones KL. Birth outcomes in pregnant women taking fluoxetine. New England Journal of Medicine, Vol. 335, No. 14, 1996.
Chia SE, Shi LM. Review of recent epidemiological studies on paternal occupations and birth defects. Occup Environ Med. 2002;59:149-155.
Cordier S, Chevrier C, Robert-Gnansia E, Lorente C, Brula C, Hours M. Risk of congenital anomalies in the vicinity of municipal solid waste incinerators. Occup Environ Med, Vol. 61, 2004.
Cragan JD, Martin ML, Waters GD, Khoury MJ. Increased risk of small intestinal atresia among twins in the United States. Arch Pediatr Adolesc Med 1994;148:733-739.
Cragan JD, Martin ML, Moore Ca, Khoury MJ. Descriptive epidemiology of small intestine atresia, Atlanta, Georgia. Teratology 1993;48:441-450.
Czeizel A. A case-control analysis of the teratogenic effects of co-trimoxazole. Reprod Toxicol 1990;4:305-313.
Czeizel AE, Toth M, Rockenbauer M. Population-based case control study of folic acid supplementation during pregnancy. Teratology 1996;53:345-351.
Czeizel AE, Rockenbauer M, Sorensen HT, Olsen J. Use of cephalosporins during pregnancy and in the presence of congenital abnormalities: a population-based, case-control study. Am J Obstet Gynecol 2001a;184:1289-1296.
Czeizel AE, Rockenbauer M, Sorensen HT, Olsen J. A population-based case-control teratologic study of ampicillin treatment during pregnancy. Am J Obstet Gynecol 2001b;185:140-147.
Doray B, Becmeur F, Girard-Lemaire F, Schluth C, Flori E. Esophageal and duodenal atresia in a girl with 12q24.3-qtr deletion. Clinical Genetics, Vol. 61, 2002.
Eros E, Czeizel AE, Rockenbauer M, Sorensen HT, Olsen J. A population-based case-control teratologic study of nitrazepam, medazepam, tofisopam, alprazolum and clonazepam treatment during pregnancy. Eur J Obstet Gynecol Reprod Biol 2002;101:147-154.
Fairbanks TJ, Kanard R, Del Moral PM, Sala FG, De Langhe S, Warburton D, Anderson KD, Bellusci S, Burns RC. Fibroblast growth factor receptor 2 IIIb invalidation—a potential cause of familial duodenal atresia. Journal of Pediatric Surgery, Vol. 39, No. 6, 2003.
Fairbanks TJ, Kanard RC, De Langhe SP, Sala FG, Del Moral PM, Warburton D, Anderson KD, Bellusci S, Burns RC. A genetic mechanism for cecal atresia: the role of the Fgf10 signaling pathway. Journal of Surgical Research, Vol. 120, 2004.
Forrester MB , Merz RD. Population-based study of small intestinal atresia and stenosis, Hawaii, 1986-2000. Public Health, Vol. 118, 2004.
Francannet C, Robert E. Etude epidemiologique des atresias intestinales: Registre Centre-Est 1976-1992. J Gynecol Obstet Biol Reprod ( Paris) 1996;25:485-494.
Fried, P. The consequences of marijuanta use during pregnancy: a review of the human literature. In Women and Cannabis: Medicine, Science, and Sociology, Haworth Integrative Healing Press.
Garne E, Rasmussen L, Husby S. Gastrointestinal malformations in Funen County, Denmark – epidemiology, associated malformations, surgery and mortality. Eur J Pediatr Surg 2002;12:101-106.
Gahukamble DB, Adnan ARM, Al-Gadi M. Distal foregut atresias in consecutive siblings and twins in the same family. Pediatr Surg Int, Vol. 19, 2003.
Gahukamble DB, Adnan ARM, Al-Gadi M. Atresias of the gastrointestinal tract in an inbred, previously unstudied population. Pediatr Surg Int, Vol. 18, 2002.
Garza JJ, Jaksic T. Intestinal atresia, stenosis, and webs. Web reference, http://www.emedicne.com/ped/topic.3043.htm. Accessed August 4, 2005.
Haeusler MC, Berghold A, Stoll C, Barisic I, Clementi M. Prenatal ultrasonographic detection of gastrointestinal obstruction: results from 18 European congenital anomaly registries. Prenat Diagn 2002;22:616-623.
Harris J, Kallen B, Robert E. Descriptive epidemiology of alimentary tract atresia. Teratology 1995;52:15-29.
Harrison RM. Hazardous waste landfill sites and congenital anomalies. Occup Environ Med, Vol. 60, 2003.
Holmes LB, Harvey EA, Coull BA, Huntington KB, Khoshbin S, Hayes AM, Ryan LM. The teratogenicity of anticonvulsant drugs. New England Journal of Medicine, Vol. 334, 2001.
Hoyme HE, Jones KL, Dixon SD, Jewett T, Hanson JW, Robinson LK, Msall ME, Allanson JE. Prenatal cocaine exposure and fetal vascular disruption. Pediatrics 1990;85:743-747.
Jones KL. Smith’s Recognizable Patterns of Human Malformation. WB Saunders, Philadelphia, 1988, p.755.
Kallen B, Mastroiacovo P, Robert E. Major congenital malformations in Down syndrome. Am J Med Genet 1996;65:160-166.
Kallen B. Congenital malformations in twins: a population study. Acta Genet Med Gemellol (Roma) 1986;35:167-178.
Khoury MJ, Becerra JE, d’Almada PJ. Maternal thyroid disease and risk of birth defects in offspring: a population-based case-control study. Paediatr Perinat Epidemiol 1989;3:402-420.
Khoury MJ, Erickson JD, Cordero JF, McCarthy BJ. Congenital malformations and intrauterine growth retardation: a population study. Pediatrics 1988;82:83-90.
Kristensen P, Irgens LM, Andersen A, Bye AS, Sundheim L. Birth defects among offspring of Norwegian farmers, 1967-1991.Epidemiology 1997;8:537-544.
Lapunzina P, Camelo JSL, Rittler M, Castilla EE. Risks of congenital anomalies in larger for gestational age infants. Journal of Pediatrics, Vol. 140, No. 2, 2002.
Martinez-Frias ML, Castilla EE, Bermejo E, Prieto L, Orioli IM. Isolated small intestinal atresias in Latin America and Spain: Epidemiological analysis. Am J Med Genet 2000;93:355-359.
Mastroiacovo P, Castilla EE, Arpino C, Botting B, Cocchi G, Goujard J, Marinacci C, Merlob P, Metneki J, Mutchinick O, Ritvanen A, Rosano A. Congenital malformations in twins: an international study. Am J Med Genet 1999;83:117-124.
Mili F, Edmonds LD, Khoury MJ, McClearn AB. Prevalence of birth defects among low-birth-weight infants. A population study. Am J Dis Child 1991;145:1313-1318.
Papp Z, Toth-Pal E, Papp C, Toth Z, Szabo M, Veress L, Torok O. Impact of prenatal mid-trimester screening on the prevalence of fetal structural anomalies: a prospective epidemiological study. Ultrasound Obstet Gynecol 1995;6:320-326.
Park-Wyllie L, Mazzotta P, Pastuszac A, Moretti ME, Beique L, Hunnisett L, Friesen MH, Jacobson S, Kasapinovic S, Chang D, Diav-Citrin O, Chitayat D, Nulman I, Einarson TR, Koren G. Birth defects after maternal exposure to corticosteroids: prospective cohort study and meta-analysis of epidemiological studies. Teratology, Vol. 62, 2000.
Ramos-Arroyo MA. Birth defects in twins: study in a Spanish population. Acta Genet Med Gemellol (Roma) 1991;40:337-344.
Rasmussen SA, Moore CA, Paulozzi LJ, Rhodenhiser EP. Risk for birth defects among premature infants: A population-based study. J Pediatr 2001;138:668-673.
Rittler M, Liascovich R, Lopez-Camelo J, Castilla EE. Parental consanguinity in specific types of congenital anomalies. Am J Med Genet 2001;102:36-43.
Rittler M, Lopez-Camelo J, Castilla EE. Sex ratio and associated risk factors for 50 congenital anomaly types: lues for causal heterogeneity. Birth Defects Research (Part A), Vol. 70, 2004.
Sencan A, Mir E, Gunsar C, Akcora B. Symptomatic annular pancreas in newborns. Med Sci Monit 2002;8:CR434-CR437.
Shaw GM, Carmichael SL, Nelson V. Congenital malformations in offspring of Vietnamese women in California, 1985-97. Teratology 2002;65:121-124.
Sorenson HT, Czeizel AE, Rockenbauer M, Steffensen FH, Olsen J. The risk of limb deficiencies and other congenital abnormalities in children exposed in utero to calcium channel blockers. Acta Obstet Gynecol Scand, Vol. 80, 2001.
Stoll C, Alembik Y, Dott B, Roth MP. Evaluation of prenatal diagnosis of congenital gastro-intestinal atresias. Eur J Epidemiol 1996;12:611-616.
Texas Department of State Health Services. Texas birth defects registry report of birth defects among 1999-2002 deliveries. 2005.
Torfs CP, Christianson RE. Anomalies in Down syndrome individuals in a large population-based registry. Am J Med Genet 1998;77:431-438.
Van Bokhoven H, Celli J, van Reeuwijk J, Rinne T, Glaudemans B, van Beusekom E, Rieu P, Newbury-Ecob RA, Chiang C, Brunner HG. MYCN haploinsufficiency is associated with reduced brain size and intestinal atresias in Feingold syndrome. Nature Genetics, Vol. 37, No. 5, 2005.
van der Pol JG, Wolf H, Boer K, Treffers PE, Leschot NJ, Hey HA, Vos A. Jejunal atresia related to the use of methylene blue in genetic amniocentesis in twins. Br J Obstet Gynaecol 1992;99:141-143.
Werler MM, Sheehan JE, Mitchell AA. Association of vasoconstrictive exposures with risks of gastroschisis and small intestinal atresia. Epidemiology, Vol. 14, 2003.
Werler MM, Sheehan JE, Mitchell AA. Maternal medication use and risks of gastroschisis and small intestinal atresia. Am J Epidemiol 2002;155:26-31.
Yamanaka S, Tanaka Y, Kawataki M, Ijiri R, Imaizumi K, Kurahasi H. Chromosome 22q11 deletion complicated by dissecting pulmonary arterial aneurysm and jujunal atresia in an infant. Arch Pathol Lab Med, Vol. 124, 2000.
Yang J, Carmichael SL, Kaidarova Z, Shaw GM. Risks of selected congenital malformations among offspring of mixed race-ethnicity. Birth Defects Research (Part A): Clinical and Molecular Teratology, Vol. 70, 2004.
Please Note: The primary purpose of this report is to provide background necessary for conducting cluster investigations. It summarizes literature about risk factors associated with this defect. The strengths and limitations of each reference were not critically examined prior to inclusion in this report. Consumers and professionals using this information are advised to consult the references given for more in-depth information. This report is for information purposes only and is not intended to diagnose, cure, mitigate, treat, or prevent disease or other conditions and is not intended to provide a determination or assessment of the state of health. Individuals affected by this condition should consult their physician and when appropriate, seek genetic counseling.
Document E58-10957 Revised November 2005